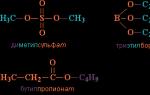
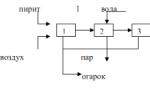
Азотистая кислота. Химические и физические свойства. Соли аммония Характер химической связи азотистой кислоты
HNO3, кислородосодержащая одноосновная сильная кислота. Твёрдая азотная кислота образует две кристаллические модификации с моноклинной и ромбической решётками.
Азотная кислота смешивается с водой в любых соотношениях. В водных растворах она практически полностью диссоциирует на ионы.
Получается при каталитическом окислении синтетического аммиака на платино-родиевых катализаторах (метод Габера) до смеси оксидов азота (нитрозных газов), с дальнейшим поглощением их водой
4NH3 + 5O2 (Pt) > 4NO + 6H2O
2NO + O2 > 2NO2 4NO2 + O2 + 2H2O > 4HNO3 Концентрация полученной таким методом азотной кислоты колеблется, в зависимости от технологического оформления процесса от 45 до 58 %. Впервые азотную кислоту получили алхимики, нагревая смесь селитры и железного купороса:
4KNO3 + 2(FeSO4 7H2O) (t°) > Fe2O3 + 2K2SO4 + 2HNO3^ + NO2^ + 13H2O
Чистую азотную кислоту получил впервые Иоганн Рудольф Глаубер, действуя на селитру концентрированной серной кислотой:
KNO3 + H2SO4(конц.) (t°) > KHSO4 + HNO3^
Дальнейшей дистилляцией может быть получена т. н. «дымящая азотная кислота», практически не содержащая воды.
Применение:
в производстве минеральных удобрений;
в военной промышленности;
в фотографии - подкисление некоторых тонирующих растворов;
в станковой графике - для травления печатных форм (офортных досок, цинкографических типографских форм и магниевых клише).
1.Разбавленная азотная кислота проявляет все свойства сильных кислот, в водных растворах она диссоциирует по следующей схеме:
HNO3 H+ + NO3–,
безводная кислота:
2HNO3® NO2+ + NO3–+ H2O.
Постепенно, особенно на свету или при нагревании азотная кислота разлагается, при хранении раствор становится коричневатым из-за диоксида азота:
4HNO3 4NO2 + 2H2O + O2.
2.Азотная кислота взаимодействует почти со всеми металлами. Разбавленная азотная кислота со щелочными и щелочноземельными металлами, а также с железом и цинком образует соответствующие нитраты, нитрат аммония или гемиоксид азота в зависимости от активности металла и воду:
4Mg + 10HNO3® 4Mg(NO3)2 + N2O + 5H2O,
С тяжелыми металлами разбавленная кислота образует соответствующие нитраты, воду и выделяется оксид азота, а в случае более сильного разбавления азот:
5Fe + 12HNO3(оч. разб.)®5Fe(NO3)3 + N2+ 6H2O,
3Cu + 8HNO3® 3Cu(NO3)2 + 2NO + 4H2O.
Концентрированная азотная кислота при взаимодействии со щелочными и щелочными металлами образует соответствующие нитраты, воду и выделяется гемиоксид азота:
8Na + 10HNO3® 8NaNO3 + N2O + 5H2O.
Такие металлы как железо, хром, алюминий, золото, платина, иридий, тантал концентрированная кислота пассивирует, т.е. на поверхности металла образуется пленка оксидов не проницаемая для кислоты. Другие тяжелые металлы при взаимодействии с концентрированной азотной кислотой образуют соответствующие нитраты, воду и выделяется оксид или диоксид азота:
3Hg + 8HNO3(хол.)®3Hg(NO3)2 + 2NO + 4H2O,
Hg + 4HNO3(гор.)®Hg(NO3)2 + 2NO2+ 2H2O,
Ag + 2HNO3® AgNO3 + NO2+ 2H2O.
3.Азотная кислота способна растворить золото, платину и другие благородные металлы, но в смеси с соляной кислотой. Их смесь в отношении три объема концентрированной соляной кислоты и один объем концентрированной азотной кислоты называют “царской водкой”. Действие царской водки заключается в том, что азотная кислота окисляет соляную до свободного хлора, который соединяется с металлами:
HNO3 + HCl ® Cl2 + 2H2O + NOCl,
2NOCl ® 2NO + Cl2.
Царская водка способна растворить золото, платину, родий, иридий и тантал, которые не растворяются ни в азотной, а уж тем более соляной кислоте:
Au + HNO3 + 3HCl ® AuCl3 + NO + 2H2O,
HCl + AuCl3® H;
3Pt + 4HNO3 + 12HCl ® 3PtCl4 + 4NO + 8H2O,
2HCl + PtCl4® H2.
4.Неметаллы также окисляются азотной кислотой до соответствующих кислот, разбавленная кислота выделяет оксид азота:
3P + 5HNO3 + 2H2O ® 3H3PO4 + 5NO ,
концентрированная кислота выделяет диоксид азота:
S + 6HNO3® H2SO4 + 6NO2+ 2H2O,
зотная кислота способна также окислять некоторые неорганические соединения:
3H2S + 8HNO3® 3H2SO4 + 8NO + 4H2O.
HNO2 - слабая одноосновная кислота, существует только в разбавленных водных растворах, окрашенных в слабый голубой цвет, и в газовой фазе. Соли азотистой кислоты называются нитритами или азотистокислыми. Нитраты гораздо более устойчивы, чем HNO2, все они токсичны.
В газовой фазе планарная молекула азотистой кислоты существует в виде двух конфигураций цис- и транс-. При комнатной температуре преобладает транс-изомер
Хим. св-ва
В водных растворах существует равновесие:
2HNO2 - N2O3 + H2O - NO^ + NO2^ + H2O
При нагревании раствора азотистая кислота распадается с выделением NO и NO2:
3HNO2 - HNO3 + 2NO^ + H2O.
HNO2 немного сильнее уксусной кислоты. Легко вытесняется более сильными кислотами из солей:
H2SO4 + Ba(NO2)2 > BaSO4v + HNO2.
Азотистая кислота проявляет как окислительные, так и восстановительные свойства. При действии более сильных окислителей (Н2О2, КМпО4) окисляется в HNO3:
2HNO2 + 2HI > 2NO^ + I2v + 2H2O;
5HNO2 + 2HMnO4 >2Mn(NO3)2 + HNO3 + 3H2O;
HNO2 + Cl2 + H2O > HNO3 + 2HCl.
Азотистая кислота применяется для диазотирования первичных ароматических аминов и образования солей диазония. Нитриты применяются в органическом синтезе при производстве органических красителей.
Получение:
N2O3 + H2O 2HNO2,
NaNO2 + H2SO4 (0° C)® NaHSO4 + HNO2
AgNO2 + HCl ® AgCl + HNO2
Свойства солей
Все нитраты хорошо растворимы в воде. С повышением температуры их растворимость сильно увеличивается. При нагревании нитраты распадаются с выделением кислорода. Нитраты аммония, щелочных и щелочноземельных металлов называют селитрами, например NaNO3 - натриевая селитра (чилийская селитра), KNO3 - калиевая селитра, NH4NO3 - аммиачная селитра. Нитраты получают действием азотной кислоты HNO3 на металлы, оксиды, гидроксиды, соли. Практически все нитраты хорошо растворимы в воде.
Нитраты устойчивы при обычной температуре. Они обычно плавятся при относительно низких температурах (200-600°C), зачастую с разложением.
Нитраты щелочных металлов разлагаются до нитритов с выделением кислорода (а при длительном нагревании ступенчато разлагаются на оксид металла, молекулярные азот и кислород, ввиду чего являются хорошими окислителями).
Нитраты металлов средней активности разлагаются при нагревании до оксидов металлов с выделением диоксида азота и кислорода.
Нитраты самых малоактивных металлов (благородные металлы) разлагаются в основном до свободных металлов с выделением диоксида азота и кислорода.
Нитраты являются достаточно сильными окислителями в твёрдом состоянии (обычно в виде расплава), но практически не обладают окислительными свойствами в растворе, в отличие от азотной кислоты.
Нитрит - соль азотистой кислоты HNO2. Нитриты термически менее устойчивы, чем нитраты. Применяются в производстве азокрасителей и в медицине.
Азотистая кислота существует либо в растворе, либо в газовой фазе. Она неустойчива и при нагревании распадается в парах:
2HNO 2 «NO+NO 2 +Н 2 О
Водные растворы этой кислоты при нагревании разлагаются:
3HNO 2 «HNO 3 +H 2 O+2NO
Эта реакция обратимая, поэтому, хотя растворение NO 2 и сопровождается образованием двух кислот: 2NO 2 + Н 2 O=HNO 2 +HNO 3
практически взаимодействием NO 2 с водой получают HNO 3:
3NO 2 +H 2 O=2HNO 3 +NO
По кислотным свойствам азотистая кислота лишь немного сильнее уксусной. Соли ее называются нитритами и в отличие от самой кислоты являются устойчивыми. Из растворов ее солей можно добавлением серной кислоты получить раствор HNO 2:
Ba(NO 2) 2 +H 2 SO 4 =2HNO 2 +BaSO 4 ¯
На основе данных о ее соединениях предполагают два типа структуры азотистой кислоты:
которым соответствуют нитриты и нитросоединения. Нитриты активных металлов имеют структуру I типа, а малоактивных металлов - II типа. Почти все соли этой кислоты хорошо растворимы, но нитрит серебра труднее всех. Все соли азотистой кислоты ядовиты. Для химической технологии важны KNO 2 и NaNO 2 , которые необходимы для производства органических красителей. Обе соли получают из оксидов азота:
NO+NO 2 +NaOH=2NaNO 2 +Н 2 О или при нагревании их нитратов:
KNO 3 +Pb=KNO 2 +PbO
Pb необходим для связывания выделяющегося кислорода.
Из химических свойств HNO 2 сильнее выражены окислительные, при этом сама она восстанавливается до NO:

Однако можно привести много примеров таких реакций, где азотистая кислота проявляет восстановительные свойства:

Определить присутствие азотистой кислоты и ее солей в растворе можно, если прибавить раствор иодида калия и крахмала. Нитрит-ион окисляет анион иода. Эта реакция требует присутствия Н + , т.е. протекает в кислой среде.
Азотная кислота
В лабораторных условиях азотную кислоту можно получить действием концентрированной серной кислоты на нитраты:
NaNO 3 +H 2 SO 4(к) =NaHSO 4 +HNO 3 Реакция протекает при слабом нагревании.
Получение азотной кислоты в промышленных масштабах осуществляется каталитическим окислением аммиака кислородом воздуха:
1. Вначале смесь аммиака с воздухом пропускают над платиновым катализатором при 800°С. Аммиак окисляется до оксида азота (II):
4NH 3 + 5O 2 =4NO+6Н 2 О
2 . При охлаждении происходит дальнейшее окисление NO до NO 2: 2NO+O 2 =2NO 2
3. Образующийся оксид азота (IV) растворяется в воде в присутствии избытка О 2 с образованием HNO 3: 4NO 2 +2Н 2 O+O 2 =4HNO 3
Исходные продукты - аммиак и воздух - тщательно очищают от вредных примесей, отравляющих катализатор (сероводород, пыль, масла и т.п.).
Образующаяся кислота является разбавленной (40-60% -ной). Концентрированную азотную кислоту (96-98% -ную) получают перегонкой разбавленной кислоты в смеси с концентрированной серной кислотой. При этом испаряется только азотная кислота.
Физические свойства
Азотная кислота - бесцветная жидкость, с едким запахом. Очень гигроскопична, «дымит» на воздухе, т.к. ее пары с влагой воздуха образуют капли тумана. Смешивается с водой в любых соотношениях. При -41,6°С переходит в кристаллическое состояние. Кипит при 82,6°С.
В HNO 3 валентность азота равна 4, степень окисления +5. Структурную формулу азотной кислоты изображают так:
Оба атома кислорода, связанные только с азотом, равноценны: они находятся на одинаковом расстоянии от атома азота и несут каждый по половинному заряду электрона, т.е. четвертая часть азота разделена поровну между двумя атомами кислорода.
Электронную структуру азотной кислоты можно вывести так:
1. Атом водорода связывается с атомом кислорода ковалентной связью:
2. За счет неспаренного электрона атом кислорода образует ковалентную связь с атомом азота:
3. Два неспаренных электрона атома азота образуют ковалентную связь со вторым атомом кислорода:
4. Третий атом кислорода, возбуждаясь, образует свободную 2р- орбиталь путем спаривания электронов. Взаимодействие неподеленной пары азота со свободной орбиталью третьего атома кислорода приводит к образованию молекулы азотной кислоты:
Химические свойства
1. Разбавленная азотная кислота проявляет все свойства кислот. Она относится к сильным кислотам. В водных растворах диссоциирует:
HNO 3 «Н + +NO - 3 Под действием теплоты и на свету частично разлагается:
4HNO 3 =4NO 2 +2Н 2 O+O 2 Поэтому хранят ее в прохладном и темном месте.
2. Для азотной кислоты характерны исключительно окислительные свойства. Важнейшим химическим свойством является взаимодействие почти со всеми металлами. Водород при этом никогда не выделяется. Восстановление азотной кислоты зависит от ее концентрации и природы восстановителя. Степень окисления азота в продуктах восстановления находится в интервале от +4 до -3:
HN +5 O 3 ®N +4 O 2 ®HN +3 O 2 ®N +2 O®N +1 2 O®N 0 2 ®N -3 H 4 NO 3
Продукты восстановления при взаимодействии азотной кислоты разной концентрации с металлами разной активности приведены ниже в схеме.

Концентрированная азотная кислота при обычной температуре не взаимодействует с алюминием, хромом, железом. Она переводит их в пассивное состояние. На поверхности образуется пленка оксидов, которая непроницаема для концентрированной кислоты.

3. Азотная кислота не реагирует с Pt, Rh, Ir, Та, Au. Платина и золото растворяются в «царской водке» - смеси 3 объемов концентрированной соляной кислоты и 1 объема концентрированной азотной кислоты:
Au+НNO 3 +3НСl= AuСl 3 +NO+2Н 2 О НСl+AuСl 3 =H
3Pt+4HNO 3 +12НСl=3PtCl 4 +4NO+8H 2 O 2HCl+PtCl 4 =H 2
Действие «царской водки» заключается в том, что азотная кислота окисляет соляную до свободного хлора:
HNO 3 +HCl=Сl 2 +2Н 2 О+NOCl 2NOCl=2NO+Сl 2 Выделяющийся хлор соединяется с металлами.
4. Неметаллы окисляются азотной кислотой до соответствующих кислот, а она в зависимости от концентрации восстанавливается до NO или NO 2:
S+бНNO 3(конц) =H 2 SO 4 +6NO 2 +2Н 2 ОР+5НNO 3(конц) =Н 3 РO 4 +5NO 2 +Н 2 О I 2 +10HNO 3(конц) =2HIO 3 +10NO 2 +4Н 2 О 3Р+5HNO 3(p азб) +2Н 2 О= 3Н 3 РО 4 +5NO
5. Она также взаимодействует с органическими соединениями.
Соли азотной кислоты называются нитратами, представляют собой кристаллические вещества, хорошо растворимые в воде. Их получают при действии HNO 3 на металлы, их оксиды и гидроксиды. Нитраты калия, натрия, аммония и кальция называются селитрами. Селитры используются главным образом как минеральные азотные удобрения. Кроме того, KNO 3 применяют для приготовления черного пороха (смесь 75% KNO 3 , 15% С и 10% S). Из NH 4 NO 3 , порошка алюминия и тринитротолуола изготавливают взрывчатое вещество аммонал.
Соли азотной кислоты при нагревании разлагаются, причем продукты разложения зависят от положения солеобразующего металла в ряду стандартных электродных потенциалов:

Разложение при нагревании (термолиз) - важное свойство солей азотной кислоты.
2KNO 3 =2KNO 2 +O 2
2Cu(NO 3) 2 =2CuO+NO 2 +O 2
Соли металлов, расположенных в ряду левее Mg, образуют нитриты и кислород, от Mg до Cu - оксид металла, NO 2 и кислород, после Си - свободный металл, NO 2 и кислород.
Применение
Азотная кислота - важнейший продукт химической промышленности. Большие количества расходуются на приготовление азотных удобрений, взрывчатых веществ, красителей, пластмасс, искусственных волокон и др. материалов. Дымящая
азотная кислота применяется в ракетной технике в качестве окислителя ракетного топлива.
Азотистая кислота - это одноосновная слабая кислота, которая может существовать только в разбавленных водных растворах голубого цвета и в газовой форме. Соли данной кислоты называют азотистокислым или нитритами. Они токсичны и более устойчивы, чем сама кислота. Химическая формула данного вещества выглядит так: HNO2.
Физические свойства:
1. Молярная масса равна 47 г/моль.
2. равна 27 а.е.м.
3. Плотность составляет 1,6.
4. Температура плавления равна 42 градусам.
5. Температура кипения равна 158 градусам.
Химические свойства азотистой кислоты
1. Если раствор с азотистой кислотой нагреть, то произойдет следующая химическая реакция:
3HNO2 (азотистая кислота) = HNO3 (кислота азотная) + 2NO выделяется в виде газа)+ H2O (вода)
2. В водных растворах диссоциирует и легко вытесняется из солей более сильными кислотами:
H2SO4 (серная кислота) + 2NaNO2 (нитрит натрия) = Na2SO4 (сульфат натрия) + 2HNO2 (азотистая кислота)
3. Рассматриваемое нами вещество может проявлять как окислительные, так и восстановительные свойства. При воздействии на него более сильных окислителей (например: хлор, пероксид водорода H2O2, окисляется до азотной кислоты (в некоторых случаях происходит образование соли азотной кислоты):
Восстановительные свойства:
HNO2 (азотистая кислота) + H2O2 (пероксид водорода) = HNO3 (азотная кислота) + H2O (вода)
HNO2 + Cl2 (хлор) + H2O (вода) = HNO3 (кислота азотная) + 2HCl (соляная кислота)
5HNO2 (азотистая кислота)+ 2HMnO4 = 2Mn(NO3)2 (нитрат марганца, соль азотной кислоты) + HNO3 (кислота азотная) + 3H2O (вода)
Окислительные свойства:
2HNO2 (азотистая кислота)+ 2HI = 2NO (оксид кислорода, в виде газа) + I2 (йод) + 2H2O (вода)
Получение азотистой кислоты
Данное вещество можно получить несколькими способами:
1. При растворении азота оксида (III) в воде:
N2O3 (оксид азота) + H2O (вода) = 2HNO3 (азотистая кислота)
2. При растворении азота оксида (IV) в воде:
2NO3 (оксид азота) + H2O (вода) = HNO3 (азотная кислота) + HNO2 (азотистая кислота)
Применение азотистой кислоты:
- диазотирование ароматических первичных аминов;
- производство солей диазония;
- в синтезе органических веществ (например, для производства органических красителей).
Воздействие азотистой кислоты на организм
Данное вещество токсично, обладает ярким мутагенным эффектом, так как по сути своей является деаминирующим агентом.
Что такое нитриты
Нитриты - это различные соли азотистой кислоты. К воздействию температур они менее устойчивы, чем нитраты. Необходимы при производстве некоторых красителей. Применяются в медицине.
Особенное значение приобрел для человека нитрит натрия. Это вещество имеет формулу NaNO2. Используется в качестве консерванта в пищевой промышленности при производстве изделий из рыбы и мяса. Представляет собой порошок чистого белого или слегка желтоватого цвета. Нитрит натрия гигроскопичен (исключение составляет очищенный нитрит натрия) и хорошо растворяется в H2O (воде). На воздухе способен постепенно окислиться до имеет сильные восстановительные свойства.
Натрия нитрит применяется в:
- химическом синтезе: для получения диазо-аминных соединений, для дезактивирования избытка натрия азида, для получения кислорода, натрия оксида и натрия азота, для поглощения углекислого газа;
- в производстве пищевых продуктов (пищевая добавка Е250): в качестве антиокислителя и антибактериального агента;
- в строительстве: в качестве противоморозной добавки к бетону в изготовлении конструкций и строительных изделий, в синтезе органических веществ, в роли ингибитора коррозии атмосферной, в производстве каучуков, попперсов, раствора добавки для взрывчатых веществ; при обработке металла для снятия слоя олова и при фосфатировании;
- в фотографии: как антиокислитель и реагент;
- в биологии и медицине: сосудорасширяющее, спазмолитическое, слабительное, бронхолитическое; как антидот при отравлении животного или человека цианидами.
В настоящее время также используются и другие соли азотистой кислоты (например, нитрит калия).
Азотистая кислота
HNO 2 - слабая одноосновная кислота, существует только в разбавленных водных растворах.
Соли азотистой кислоты называются нитритами. Нитриты гораздо более устойчивы, чем HNO 2 , все они токсичны.
Получение:
1. N 2 O 3 + H 2 O = 2HNO 2
Как можно еще получить азотистую кислоту? ()
Какая степень окисления в азотистой кислоте?
Значит, кислота проявляет как окислительные, так и восстановительные свойства.
При действии более сильных окислителей окисляется в HNO 3:
5HNO 2 +2HMnO 4 → 2Mn(NO 3) 2 + HNO 3 + 3H 2 O;
HNO 2 + Cl 2 + H 2 O → HNO 3 + 2HCl.
2HNO 2 + 2HI → 2NO + I 2 ↓ + 2H 2 O – восстановительные свойства
Качественная реакция на нитрит-ион NO 2 – – взаимодействие нитритов с раствором йодида калия КI, подкисленным разбавленной серной кислотой.
Как должна изменить окраску йодкрахмальная бумажка под действием свободного I 2 ?

Получение солей (нитратов и нитритов)
Назовите способы получения солей, которые вам известны? Как можно получить нитраты и нитриты?
1) Металл + неметалл = соль;
2) металл + кислота = соль + водород;
3) оксид металла + кислота = соль + вода;
4) гидроксид металла + кислота = соль + вода;
5) гидроксид металла + кислотный оксид = соль + вода;
6) оксид металла + оксид неметалла = соль;
7) соль 1 + гидроксид металла (щелочь) = соль 2 + гидроксид металла (нерастворимое основание);
8) соль 1 + кислота (сильная) = соль 2 + кислота (слабая);
9) соль 1 + соль 2 = соль 3 + соль 4
10) соль 1 + металл (активный) = соль 2 + металл (менее активный).
Специфический способ получения нитратов и нитритов:

диспропорционирование.
В присутствии избытка кислорода

Соли азотной кислоты – нитраты
нитраты щелочных металлов, кальция, аммония – селитры
KNO 3 - калийная селитра,
NH 4 NO 3 - аммиачная селитра.
Физические свойства:
Все нитраты твёрдые кристаллические вещества, белого цвета, хорошо растворимые в воде. Ядовиты!
Химические свойства нитратов
Взаимодействие нитратов с металлами, кислотами, щелочами, солями
Задание . Отметить признаки каждой реакции, записать молекулярные и ионные уравнения, соответствующие схемам:
Cu(NO 3) 2 + Zn… ,
AgNO 3 + HCl… ,
Cu(NO 3) 2 + NaOH… ,
AgNO 3 + BaCl 2 … .
Разложение нитратов
При нагревании твердых нитратов все они разлагаются с выделением кислорода (исключением является нитрат аммония), при этом их можно разделить на три группы.
Первую группу составляют нитраты щелочных металлов
2КNО 3 = 2КNО 2 + О 2 .
Вторую группу от щелочноземельных металлов до меди включительно
2Сu(NО 3) 2 = 2СuО + 4NО 2 + O 2 ,
Третью группу Ме после Сu
Hg(NО 3) 2 = Нg + 2NО 2 + О 2 ,
Почему азота в природе много (он входит в состав атмосферы), а растения часто дают плохой урожай из-за азотного голодания? (Растения не могут усваивать молекулярный азот из воздуха. При недостатке азота задерживается образование хлорофилла, задерживается рост и развитие растения.)
Назовите способы усвоения атмосферного азота.
(Часть связанного азота поступает в почву во время гроз. Бобовые, на корнях которых развиваются клубеньковые бактерии, способные связывать атмосферный азот, переводя его в соединения, доступные для растений.)
Снимая урожаи, человек ежегодно уносит вместе с ними огромные количества связанного азота. Эту убыль он покрывает внесением не только органических, но и минеральных удобрений (нитратных, аммиачных, аммонийных). Азотные удобрения вносят под все культуры. Азот усваивается растениями в виде катиона аммония и нитрат-аниона NO 3 – .
Доклады учеников
Влияние нитратов на окружающую среду и организм человека
Первая помощь при отравлении нитратами
Причины накопления нитратов в овощах и способы выращивания экологически чистой продукции растениеводства
Азотистая кислота HN0 2 известна лишь в разбавленных растворах. Она неустойчива, поэтому в чистом виде не существует. Формула азотистой кислоты может быть представлена в виде двух таутомерных форм:
Нитрит-ион N0 2 имеет угловую форму:

При нагревании азотистая кислота расщепляется:
Азот в азотистой кислоте имеет степень окисления +3, что соответствует промежуточному состоянию между наивысшей (+5) и низшей (-3) степенями окисления. Поэтому азотистая кислота проявляет как окислительные, так и восстановительные свойства.
Окислитель:
Восстановитель:
![]()
Соли азотистой кислоты - нитриты - являются устойчивыми соединениями и за исключением AgN0 2 легко растворимы в воде. Как и сама азотистая кислота, нитриты обладают окислительно-восстановительными свойствами.
Окислитель:
Восстановитель:
Реакция с KI в кислой среде находит широкое применение в аналитической химии для обнаружения нитрит-иона N0 2 (выделяющийся свободный иод окрашивает раствор крахмала).
Большинство солей азотистой кислоты ядовиты. Наибольшее применение имеет нитрит натрия NaN0 2 , который широко используют в производстве органических красителей, лекарственных веществ, в аналитической химии. В медицинской практике применяется как сосудорасширяющее средство при стенокардии.
Азотную кислоту HN0 3 в лабораторных условиях можно получить действием концентрированной серной кислоты на NaN0 3:
Азотную кислоту в промышленных масштабах получают каталитическим окислением аммиака кислородом воздуха. Этот метод получения HN() 3 состоит из нескольких стадий. Вначале смесь аммиака с воздухом пропускают над платиновым катализатором при 800°С. Аммиак при этом окисляется до NO:
При охлаждении происходит дальнейшее окисление NO до N0 2:
![]()
Образующийся N0 2 растворяется в воде с образованием HN0 3:
Чистая азотная кислота - это бесцветная жидкость, которая при 42°С переходит в кристаллическое состояние. На воздухе она «дымит», так как пары ее с влагой воздуха образуют мелкие капельки тумана. С водой смешивается в любых соотношениях. HN0 3 имеет плоское строение:

Азот в HN0 3 является однозарядным и четырехковалентным. Нитрат- ион N0 3 имеет форму плоского треугольника, что объясняется ^-гибридизацией валентных орбиталей азота:

Азотная кислота относится к числу наиболее сильных кислот. В водных растворах она полностью диссоциирована на ионы Н + и N0 3 .
Для азотной кислоты характерны исключительно окислительные свойства. Азот в азотной кислоте находится в состоянии наивысшего окисления +5, поэтому он может только присоединять электроны. Уже под влиянием света азотная кислота разлагается с выделением N0 2 и 0 2:
В зависимости от концентрации азотной кислоты и природы восстановителя образуются различные продукты, где азот проявляет степень окисления от +4 до
Концентрированная азотная кислота окисляет большинство металлов (кроме золота и платины).
При взаимодействии концентрированной HN0 3 с малоактивными металлами, как правило, образуется N0 2:
Однако разбавленная азотная кислота в этом случае восстанавливается до NO:
Если в реакцию окисления с разбавленной азотной кислотой вступают более активные металлы, то выделяется N 3 0:
Очень разбавленная азотная кислота при взаимодействии с активными металлами восстанавливается до солей аммония:
Железо легко взаимодействует с разбавленной азотной кислотой и не реагирует на холоде с концентрированной. Аналогично ведут себя хром и алюминий. Объясняется это тем, что на поверхности этих металлов образуются оксидные пленки, которые и тормозят дальнейшее окисление металла (пассивация металла).
Таким образом, при взаимодействии азотной кислоты с металлами водород не выделяется.
Неметаллы при нагревании с HN0 3 окисляются до кислородных кислот. В зависимости от концентрации азотная кислота восстанавливается до N0 2 или NO:

Смесь, состоящая из одного объема азотной и трех объемов концентрированной соляной кислоты, называется царской водкой. Эта смесь - более сильный окислитель и растворяет такие благородные металлы, как золото и платину. Действие царской водки основано на том, что HN0 3 окисляет НС1 с выделением нитрозилхлорида, разлагающегося с образованием атомарного хлора и NO. Роль окислителя при взаимодействии с металлами выполняет хлор:

Взаимодействие с золотом протекает по реакции
Азотная кислота в зависимости от концентрации по-разному ведет себя по отношению к сульфидам, проявляющим восстановительные свойства. Так, разбавленная азотная кислота (до 20%) окисляет сульфид-ион S 2- до нейтральной серы, а сама восстанавливается до NO. Более концентрированная азотная кислота (30%-ный раствор) окисляет S 2 до SOf , восстанавливаясь при этом до NO:
В безводной азотной кислоте протекают следующие равновесные процессы:
Для распознавания нитрат-иона N0 3 и отличия его от нитрит-иона N0 2 пользуются несколькими реакциями:
а) нитраты в щелочной среде могут быть восстановлены до аммиака металлами - цинком или алюминием:
- (выделяющийся газообразный аммиак можно обнаружить по посинению влажной лакмусовой бумаги);
- б) сульфат железа(П) в кислой среде окисляется азотной кислотой до сульфата железа(Ш). Азотная кислота восстанавливается до NO, который с избытком FeSO^ образует комплексное соединение бурого цвета:
Соли азотной кислоты, называемые нитратами, - кристаллические вещества, хорошо растворимые в воде. При нагревании они разлагаются с выделением 0 9 . Нитраты, содержащие щелочные металлы и металлы, стоящие в ряду стандартных электродных потенциалов левее магния (включая магний), с отщеплением кислорода переходят в соответствующие нитриты:
Нитраты металлов, стоящих в ряду стандартных электродных потенциалов правее меди, расщепляются с образованием свободных металлов:
Нитраты остальных металлов разлагаются до оксидов:

Для качественного обнаружения применяется реакция
в результате которой выделяется бурый газ (N0 9).
Так как нитраты легко отщепляют кислород при высоких температурах и, следовательно, являются окислителями, то их применяют для изготовления легко воспламеняющихся и взрывчатых смесей. Например, порох представляет собой смесь состава 68% KN0 3 , 15% S и 17% С.
Наиболее важное значение имеют NaNO ;j (чилийская селитра), KN0 3 (калийная селитра), NH 4 N0 3 (аммонийная селитра) и Ca(NO:i) 2 (кальциевая селитра). Все эти соединения используются в сельском хозяйстве в качестве удобрений.
Биологическая роль азота. Азот - это макроэлемент, входит в состав аминокислот белков, РНК и ДНК, гормонов, ферментов, витаминов и многих других жизненно важных субстратов.